
据人民网11月15日电 (记者赵永新)这是全球癌症患者的福音,更是中国新药研发的里程碑:当地时间11月14日,美国食品药品监督管理局(FDA)宣布:中国企业百济神州自主研发的抗癌新药“泽布替尼”,以“突破性疗法”的身份,“优先审评”获准上市!
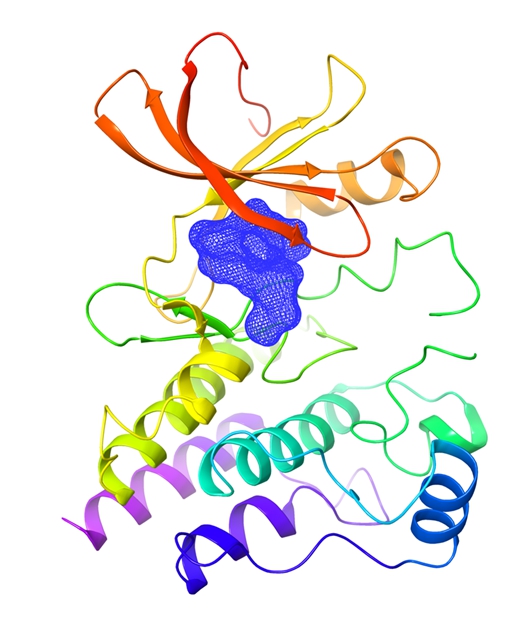
泽布替尼与BTK蛋白复合物晶体结构示意图。
由此,泽布替尼成为第一个在美获批上市的中国本土自主研发抗癌新药,堪称中国70年制药历史上的“零突破”,改写了中国抗癌药“只进不出”的尴尬历史。
百济神州的“种子选手”
说到泽布替尼,不妨先了解一下其研发公司——一贯低调的百济神州(BeiGene)。

位于北京昌平中关村生命科学园的百济神州研发大楼。
百济神州2010年创立于北京昌平的中关村生命科学园,是一家诞生于中国本土的抗癌新药研发公司。几位高管都有来头:联合创始人、科学顾问委员会主席王晓东是美国科学院院士、中国科学院外籍院士、北京生命科学研究所所长;联合创始人、董事长欧雷强是医药圈儿知名的管理专家;中国区总经理兼公司总裁,则是2018年5月从辉瑞中国区总裁位置上加盟的吴晓滨博士。

百济神州联合创始人、科学顾问委员会主席王晓东。

百济神州联合创始人、董事长欧雷强。
自成立之日起,百济神州就抱定“研发世界最好抗癌药”的决心,秉承“高质量、合规范和国际化”的原则,高举高打、闷头研发,很快成为国际新药研发领域的一匹黑马。2016年百济神州在美国纳斯达克成功上市,2018年又在香港上市,成为目前我国唯一一个境内外“双上市”的新药研发企业。如今,百济神州在中国大陆、美国、澳大利亚和瑞士拥有3000多名员工,在中国、美国、欧洲等国家和地区开展临床的产品超过10个,包括新型口服小分子靶向药物和抗体类生物制剂。与此同时,百济神州还在探索抗癌治疗的药物组合方案,旨在为癌症患者的生活带来持续、深远的影响。
其中,泽布替尼就是百济神州的 “种子选手”之一。
泽布替尼的英文名称为zanubrutinib,是以布鲁顿氏酪氨酸激酶(BTK)为靶点的新型强效抑制剂,其研发代号为BGB-3111。
“于1993年被科学家发现的BTK,是一个很好的抗肿瘤药物靶点。” 泽布替尼的主要发明人之一、百济神州化学研发负责人王志伟博士告诉记者,在泽布替尼之前,强生公司推出了以BTK为靶点的的第一代BTK抑制剂“伊布替尼”(2013年在美上市),目前适应症包括套细胞淋巴瘤、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、华氏巨球蛋白血症等,去年销售额约为62亿美元。
为进一步优化BTK抑制剂的效果,2012年7月,百济神州的BTK抑制剂开发在研究部门正式立项。“当时对于已有的BTK抑制剂,药物的选择性和吸收性是两个有待提高的关键环节。我们的设计思路是,对BTK靶点的特异性结合率最大化,实现更好疗效;同时最大程度地减少脱靶效应,以降低不良反应的发生率。” 王志伟告诉记者。
经过一系列的测试与筛选后,研究团队从最初合成的500多个化合物中,选定了最终的候选分子,并将其命名为BGB-3111。王志伟介绍说:“之所以叫这个名字,是表明它是百济神州成立之后做出的第3111个化合物。”
连获FDA特殊通道认定“四大满贯”
2013年4月,百济神州递交了BGB-3111的专利申请,这是一项从中国专利局出发的全球专利,标志着BGB-3111是不折不扣的中国本土研发抗癌新药。

百济神州北京昌平研发中心化学实验室。
2014年,百济神州在澳大利亚递交了临床试验的申请,并于当年8月完成全球首名患者给药。此时距离对BTK抑制剂的立项仅过去了2年零1个月,速度之快,充分证明了研发团队的专业水准和工作效率。
2016年7月,泽布替尼在中国进入临床试验;2017年1月,全球3期注册性临床试验启动。
据泽布替尼研发的主要领导者之一,百济神州高级副总裁汪来博士介绍,在针对多种B细胞恶性肿瘤的一系列临床试验中,泽布替尼均表现出良好的疗效及安全性,让同行看到了其成为全球同类最佳(best-in-class)药物的潜力。
汪来介绍说,比如在一项针对复发/难治性套细胞淋巴瘤(MCL) 关键性2期多中心临床试验中,经泽布替尼治疗后,由独立评审委员会评估的结果显示:患者的总体缓解率(ORR)达84%,完全缓解率(CR)高达59%。
据记者了解,全球已上市的另外两款BTK抑制剂此前针对同一适应症的临床数据分别为:伊布替尼的ORR和CR分别为68%和21%,阿卡替尼(二代BTK抑制剂,2017年在美上市)的ORR和CR分别为81%和40%。
凭借优异的临床表现,泽布替尼成为第一个获得FDA“四大满贯”的中国抗癌新药——
孤儿药认定:2016年,先后获得FDA授予3项孤儿药资格认定,分别用于治疗套细胞淋巴瘤、华氏巨球蛋白血症和慢性淋巴细胞白血病;
快速通道:2018年7月,FDA授予泽布替尼快速通道资格,用于治疗华氏巨球蛋白血症;
突破性疗法:2019年1月,FDA授予泽布替尼突破性疗法认定,用于治疗复发难治性套细胞淋巴瘤。这是中国自主研发的抗癌新药首次获得该项认定,也是FDA历史上第一次主要依靠中国研究数据授予的突破性疗法认证;
优先审评:2019年8月,FDA受理泽布替尼治疗复发难治性套细胞淋巴瘤的新药上市申请,并授予其优先审评资格
“四大满贯”中,突破性疗法认定(Breakthrough Therapy designation)的“含金量”最高。
“突破性疗法认定是美国FDA鼓励新药研发的四项激励措施之一,也是FDA支持力度最大的一项加快措施。截至9月30日,今年获得FDA授予突破性疗法认定并最终获得审批的药品只有16个。”据百济神州全球药政事务负责人闫小军介绍,在研新药能否获得FDA的突破性疗法认定,取决于两项标准:一是该药是用于治疗严重的或威胁生命的疾病;二是药物的疗效特别好。“获得突破性疗法认定,不仅代表着FDA对这一在研药物的肯定,也会显著加快候选药物的开发、审评。”
此前,强生开发的伊布替尼、百时美施贵宝开发的那武利尤单抗注射液(去年在我国获批的PD-1类免疫肿瘤药物,俗称“O药”)、阿斯利康开发的甲磺酸奥西替尼等“重磅炸弹”,都曾获得过FDA的突破性疗法认定。
近年来,中国到美国FDA申请临床试验的在研新药已有多个;截至目前,抗肿瘤药领域获得突破性疗法认定的,泽布替尼是第一个。
中国患者何时能用上泽布替尼?
“百济神州目前正在全球范围对泽布替尼开展16项临床试验研究,包括9项注册性或有望实现注册的临床试验。”据百济神州中国区总经理兼公司总裁吴晓滨博士介绍,截至目前,全球已有超过1600位患者接受了泽布替尼的临床试验治疗。

百济神州公司总裁吴晓滨。
获得FDA批准上市后,预计美国患者很快就可以用上泽布替尼了。
那么,中国患者何时能用上它?
“2018年8月、10月,国家药品监督管理局先后受理了泽布替尼针对复发/难治性套细胞淋巴瘤和复发/难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤两个适应症的新药上市申请,并纳入优先审评,目前还在审评中。”吴晓滨表示,我们期待着泽布替尼能早日在国内获准上市,以更好的疗效、更可及的价格造福肿瘤患者。